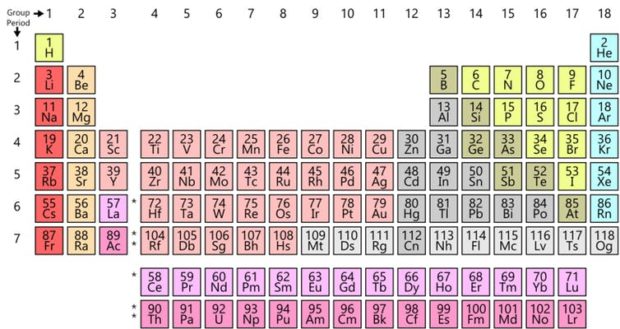
Das Periodensystem nach Dmitri Mendelejew hat 150. Geburtstag. Für die Meisten verbunden mit unangenehmen Erinnerungen an muffige Schulräume, dient es Schülern, Studenten und Wissenschaftlern heute als eine Übersicht der Elemente – und war nicht der erste Versuch, diese sinnvoll zu versammeln.
In matten Farben und mit eckigen Kästchen starrt das Periodensystem von nahezu jeder Wand der Chemielabore dieser Welt auf uns herunter. Die Version des Periodensystems, die wir heute kennen und nutzen, wurde 1869 vom russischen Chemiker Dmitri Mendelejew entwickelt, als Ergebnis seiner Bemühungen, die Elemente in ein lesbares Ordnungssystem einzugliedern.
21 Jahre zuvor hatte der britische Naturforscher John Dalton ein Tableau der 20 Elemente angelegt, die der Wissenschaft zu diesem Zeitpunkt bekannt waren. Dalton war auch als Lehrer tätig und seine Anordnung diente der Veranschaulichung für den Unterricht. Dieses Modell konnte sich nicht lange halten, da es zwar die zu dem Zeitpunkt bekannten Elemente versammelte, aber außer Acht ließ, dass Wissenschaftler in rasantem Tempo neue Elemente entdeckten.

Dem Chemiker John Newlands gelang ein neuer Ansatz. Er brachte die schlichte Auflistung in ein System, basierend auf den chemischen und physikalischen Eigenschaften der Elemente. Er stellte fest, dass das achte Element (Fluor) dem ersten (Wasserstoff) ähnelte. Auch das neunte ähnelte dem zweiten Element in seinen Eigenschaften. Er untersuchte dies weiter und erkannte eine Achter-Periodizität, die er Oktavengesetz nannte. Damit war der Grundgedanke des Periodensystems gegeben, denn periodisch ist, was in gleichen Abständen auftritt. Anders als drei Jahre später bei Mendelejew konnte aber auch seine Variante nicht mit der Geschwindigkeit der Wissenschaft mithalten.
Aber worin unterscheiden sich beide Ansätze nun genau? Es gibt keine Belege darüber, ob Mendelejew von Newlands Erkenntnissen erfuhr, jedoch sind dessen Überlegungen Grundlage seiner Arbeit, erweitert um einen genialen Gedanken: Er ließ Lücken für Elemente, die noch zu entdecken waren. Besonders erstaunlich ist dabei, dass er schon Jahre vor der Entdeckung dieser Elemente ihre Massezahlen kannte und an den passenden Plätzen in seinem Periodensystem Raum dafür ließ.

Auf den ersten Blick unterscheidet sich Mendelejews System von unserem heutigen optisch zunächst signifikant, doch dreht man es um 90 Grad, wird die Ähnlichkeit zu dem modernen Periodensystem ersichtlich. Für die Wissenschaft waren damit die Elemente erstmals sinnvoll sortiert. Sein Werk wurde von der Royal Society mit der Davy-Medaille geehrt – die höchste britische Auszeichnung für Wissenschaft auf dem Gebiet der Chemie.